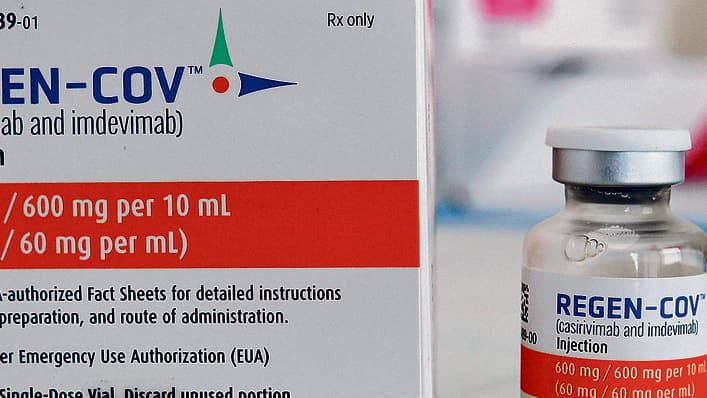
El Ministerio de Salud informó el miércoles que comprará Regeneron, un medicamento que podría salvar vidas y que supuestamente los funcionarios de salud están evitando suministrar a los israelíes que padecen síntomas de COVID-19 leves y moderados.
Luego de un informe de Ynet a principios de este mes que mostraba que el medicamento no se ofrecía a la mayoría de los pacientes debido a su alto costo, el ministerio dijo que las prestadoras de servicios de salud administrarán el Regeneron después de que se comprobara su eficacia para prevenir un deterioro y, a menudo, la muerte como resultado del virus.
Regeneron, un medicamento aprobado por la Administración de Medicamentos y Alimentos de Estados Unidos (FDA, por sus siglas en inglés) con un historial probado en ese país en reducir el número de hospitalizaciones, es un cóctel de dos anticuerpos monoclonales.
El doctor Anthony Fauci, miembro del equipo de asesores médicos del gobierno estadounidense, recomendó su uso el mes pasado. "Queremos que las personas, incluidos los médicos y los pacientes potenciales, entiendan las ventajas de esta forma muy eficaz de tratar la infección temprana", sostuvo Fauci. "Los ensayos clínicos han demostrado que el tratamiento temprano con anticuerpos monoclonales anti-SARS-CoV-2 puede reducir el riesgo de hospitalización o muerte por COVID-19 entre un 70 y un 85 por ciento", explicó.
3 צפייה בגלריה
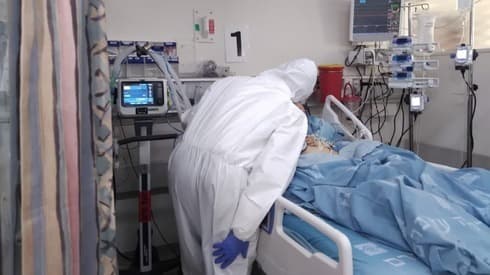

Sala de coronavirus en el Centro Médico Hadassah en Jerusalem.
(Portavoz de Hadassah)
Israel ya adquirió miles de dosis del medicamento y se administraron a cientos de pacientes con COVID, pero no estaba disponible para el público en general en todos los hospitales.
"Sólo aquellos que fueron hospitalizados con nosotros pudieron recibir el medicamento", dijo un alto funcionario de uno de los hospitales. "Algunos lo pagaron de sus propios bolsillos. Es necesario conocerlo para poder pedirlo”, agregó.
Otros altos funcionarios de salud dijeron que no entendían por qué el medicamento no estaba disponible para todos los que lo necesitaban y agregaron que una posible razón podrían ser las luchas burocráticas y desacuerdos sobre quién sería responsable de su administración.
El medicamento aún se encuentra en su etapa experimental y recibió una autorización de emergencia de la FDA. Debe administrarse en las primeras etapas de la infección y se estima que evita el deterioro hacia un cuadro grave de la enfermedad.